Đường cong chuẩn độ là công cụ quan trọng trong hóa phân tích, giúp mô tả sự thay đổi pH của dung dịch khi thêm dung dịch chuẩn vào mẫu thử. Qua biểu đồ này, các nhà khoa học có thể xác định điểm tương đương, đánh giá độ mạnh, yếu của axit và bazơ, cũng như lựa chọn chỉ thị màu phù hợp.
Đường cong chuẩn độ là gì?
Đường cong chuẩn độ là biểu đồ thể hiện sự thay đổi pH của dung dịch theo thể tích dung dịch chuẩn được thêm vào trong quá trình chuẩn độ. Thông qua đồ thị này, người phân tích có thể xác định điểm tương đương – thời điểm lượng axit và bazơ phản ứng vừa đủ với nhau.
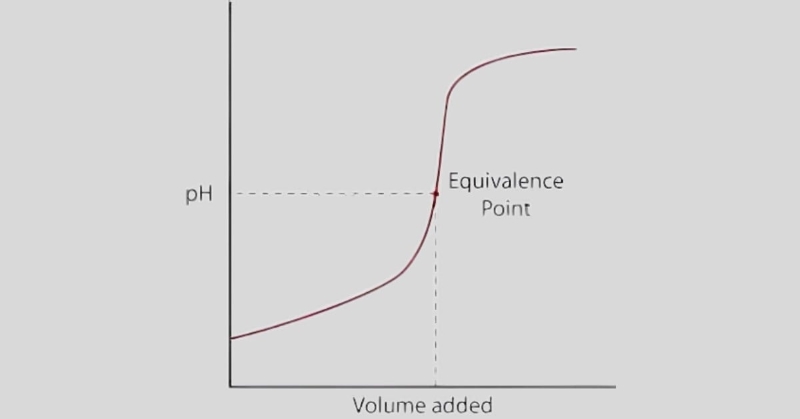
Đường cong chuẩn độ là biểu đồ thể hiện sự thay đổi pH
Trục hoành biểu diễn thể tích dung dịch chuẩn, còn trục tung thể hiện giá trị pH. Mỗi loại phản ứng (axit mạnh – bazơ mạnh, axit yếu – bazơ mạnh,…) sẽ có dạng đường cong khác nhau, phản ánh đặc trưng của từng hệ hóa học. Đường cong này không chỉ giúp chọn chỉ thị màu phù hợp mà còn hỗ trợ xác định pKa, pKb và đánh giá độ tinh khiết của dung dịch trong các thí nghiệm định lượng, sản xuất hóa chất hay kiểm định chất lượng.
Các loại đường cong chuẩn độ
Đường cong chuẩn độ được chia thành nhiều loại tùy theo bản chất phản ứng và đặc điểm của dung dịch. Phổ biến nhất là chuẩn độ axit – bazơ, trong đó pH của dung dịch thay đổi theo thể tích chất chuẩn được thêm vào. Ngoài ra, còn có chuẩn độ oxy hóa – khử, chuẩn độ tạo phức và chuẩn độ kết tủa, mỗi loại có cách biểu diễn và dạng đường cong riêng, phản ánh sự biến đổi điện thế, độ dẫn hoặc nồng độ ion trong dung dịch.
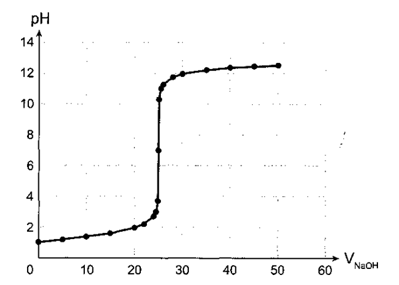
Chuẩn độ axit – bazơ phụ thuộc vào độ mạnh của các chất phản ứng
Trong chuẩn độ axit – bazơ, hình dạng đường cong phụ thuộc vào độ mạnh – yếu của các chất phản ứng. Với axit mạnh và bazơ mạnh, pH thay đổi đột ngột quanh điểm tương đương, tạo đường cong dốc rõ rệt. Ngược lại, khi axit yếu hoặc bazơ yếu tham gia, độ dốc nhỏ hơn và điểm tương đương lệch khỏi pH = 7. Ngoài ra, một số tài liệu còn phân biệt đường cong tuyến tính và đường cong logarit, dùng trong các phép chuẩn độ đặc biệt nhằm tăng độ chính xác khi phân tích nồng độ.
Cách vẽ và phân tích đường cong chuẩn độ
Để vẽ đường cong chuẩn độ chính xác, cần bắt đầu từ khâu chuẩn bị dung dịch và thiết bị. Dung dịch chuẩn (ví dụ NaOH hoặc HCl) phải có nồng độ xác định rõ ràng, trong khi mẫu thử được đo bằng pipet hoặc bình định mức để đảm bảo thể tích chính xác. Thiết bị đo pH hoặc điện cực phải được hiệu chuẩn trước khi sử dụng để kết quả đo tin cậy.
Khi tiến hành chuẩn độ, dung dịch chuẩn được thêm từ từ vào dung dịch mẫu, vừa thêm vừa khuấy đều. Sau mỗi lần thêm, ghi lại giá trị pH và thể tích tương ứng, đặc biệt chú ý khi pH thay đổi nhanh, đây là vùng gần điểm tương đương. Dữ liệu được thu thập càng dày thì đường cong vẽ ra càng chính xác.
Tiếp theo, vẽ đồ thị pH theo thể tích dung dịch chuẩn. Trục hoành biểu diễn thể tích dung dịch chuẩn đã thêm, còn trục tung thể hiện pH của dung dịch. Đồ thị thường có dạng chữ S với phần dốc đứng thể hiện sự thay đổi pH đột ngột quanh điểm tương đương.
Khi phân tích đường cong, chuyên viên xác định điểm có độ dốc lớn nhất – chính là điểm tương đương, nơi phản ứng giữa axit và bazơ hoàn toàn. Từ thể tích tại điểm này, có thể tính được nồng độ chất cần xác định dựa vào công thức chuẩn độ. Ngoài ra, hình dạng đường cong còn giúp đánh giá độ mạnh – yếu của axit hoặc bazơ, cũng như lựa chọn chỉ thị màu phù hợp cho từng phản ứng.
Ý nghĩa của đường cong chuẩn độ trong hóa học
Đường cong chuẩn độ không đơn thuần là một biểu đồ minh họa, mà là công cụ phân tích mạnh mẽ giúp các nhà khoa học và kỹ thuật viên hiểu rõ quá trình phản ứng chuẩn độ và rút ra các thông số chính xác. Đầu tiên, từ đường cong ta có thể xác định điểm tương đương, tức thể tích dung dịch chuẩn độ khi phản ứng giữa chất chuẩn và chất phân tích vừa hoàn toàn. Việc này là nền tảng để tính nồng độ chất phân tích trong mẫu thử.

Đường cong chuẩn độ còn phục vụ trong kiểm soát chất lượng và nghiên cứu phát triển.
Thứ hai, hình dạng đường cong (như độ dốc, vùng chuyển tiếp, vùng đệm) tiết lộ bản chất của phản ứng, ví dụ acid mạnh hay yếu, có hệ đệm hay không hoặc ảnh hưởng của tạp chất. Điều này cho phép người phân tích lựa chọn chỉ thị thích hợp và đảm bảo kết quả đo không bị sai lệch lớn.
Thứ ba, đường cong chuẩn độ còn phục vụ trong kiểm soát chất lượng và nghiên cứu phát triển. Trong công nghiệp hóa chất, thực phẩm, dược phẩm, môi trường… phép đo chuẩn độ và đồ thị thu được giúp đánh giá độ tinh khiết, hiệu suất phản ứng, phát hiện sự cố như dung dịch bị nhiễm bẩn hoặc thiết bị đo sai lệch.
Ứng dụng thực tế của đường cong chuẩn độ
Trong các phòng thí nghiệm và nhà máy công nghiệp, việc sử dụng đường cong chuẩn độ không chỉ dừng lại ở việc xác định nồng độ chất phân tích mà còn mở rộng sang nhiều ứng dụng quan trọng. Chẳng hạn, trong kiểm tra chất lượng nước uống hoặc xử lý nước thải, chuẩn độ axit – bazơ kèm theo đường cong giúp xác định nhanh độ kiềm, độ axit hoặc hàm lượng ion đảm bảo tuân thủ tiêu chuẩn môi trường.

Ứng dụng trong việc kiểm tra chất lượng nước uống
Ngoài ra, trong ngành dược phẩm hoặc hóa chất, xây dựng đường cong chuẩn độ được sử dụng để kiểm soát độ tinh khiết của nguyên liệu và sản phẩm trung gian. Ví dụ như xác định xem phản ứng đã hoàn tất chưa, kiểm soát sai số chuẩn độ và đảm bảo độ ổn định của sản phẩm. Còn trong giáo dục và nghiên cứu, đường cong chuẩn độ là công cụ trực quan giúp sinh viên và nhà nghiên cứu hình dung quá trình trung hòa, khảo sát phản ứng acid – bazơ, xác định hằng số cân bằng và tìm hiểu ảnh hưởng tạp chất hoặc hệ đệm.
Ví dụ minh họa đường cong chuẩn độ giữa axit mạnh và bazơ mạnh
Hãy xem xét một phép chuẩn độ mẫu, chuẩn độ HCl (axit mạnh) bằng dung dịch NaOH (bazơ mạnh) với nồng độ tương đương (ví dụ 0,1 M). Phản ứng xảy ra là:
HCl + NaOH => NaCl + H2O
Ban đầu, dung dịch HCl có pH rất thấp (thường < 2) do H+ phân li hoàn toàn. Khi tiến hành cách vẽ đường cong chuẩn độ, NaOH được thêm từ từ, pH tăng chậm cho đến gần điểm tương đương. Gần điểm tương đương, chỉ cần một lượng nhỏ NaOH thêm vào cũng làm pH tăng rất mạnh, đây là vùng dốc lớn trên đường cong.
Tại điểm tương đương, khi mol HCl ban đầu = mol NaOH đã thêm dung dịch chứa NaCl và nước và pH gần bằng 7 (nếu dung dịch loãng). Sau khi vượt điểm tương đương, NaOH dư khiến pH tăng tiếp tục, vẽ ra phần đường cong cao hơn. Trong phép chuẩn độ này, điểm tương đương nằm gần pH = 7 và đoạn chuyển rất dốc.
Nhìn chung, đường cong chuẩn độ không chỉ là biểu đồ minh họa quá trình phản ứng giữa axit và bazơ mà còn là công cụ phân tích quan trọng trong hóa học. Từ việc xác định điểm tương đương, đánh giá độ mạnh, yếu của chất phản ứng, đến kiểm soát chất lượng và nghiên cứu phát triển, đường cong này giúp nâng cao độ chính xác và hiệu quả trong thực hành.


