Chuẩn độ là phương pháp cơ bản trong hóa học phân tích, được ứng dụng rộng rãi trong thực tế, từ xác định nồng độ muối trong thực phẩm đến kiểm tra chất lượng nước sinh hoạt. Kỹ thuật này giúp xác định chính xác nồng độ chất trong dung dịch, đảm bảo kết quả tin cậy và hỗ trợ tối ưu trong sản xuất, kiểm định chất lượng và môi trường.
Chuẩn độ là gì?
Trong hóa phân tích, chuẩn độ dung dịch là gì là câu hỏi thường gặp khi nhắc đến các phương pháp định lượng cơ bản. Thực chất, đây là kỹ thuật giúp xác định chính xác nồng độ của một chất phân tích trong dung dịch thông qua việc sử dụng dung dịch chuẩn có nồng độ đã biết. Cụ thể, người ta cho dung dịch chuẩn phản ứng với dung dịch chứa chất cần xác định cho đến khi phản ứng hoàn tất; từ thể tích dung dịch chuẩn đã dùng có thể tính ra nồng độ của chất phân tích.
Kỹ thuật giúp xác định chính xác nồng độ của một chất
Vì vậy, chuẩn độ dung dịch được xem là một trong những phương pháp cổ điển nhưng vẫn giữ vai trò quan trọng hàng đầu trong hóa học hiện đại. Phương pháp này còn có tên tiếng anh là titration, nó không chỉ được ứng dụng phổ biến trong các phòng thí nghiệm mà còn trong sản xuất, kiểm định chất lượng và phân tích môi trường.
Có mấy loại chuẩn độ? Phân loại các phương pháp chuẩn độ phổ biến
Các phương pháp chuẩn độ trong hóa học được phân loại dựa trên phản ứng xảy ra và kỹ thuật thực hiện. Về phản ứng, có bốn nhóm chính. Thứ nhất là titration axit – bazơ, dựa trên phản ứng trung hòa giữa H+ và OH-, phổ biến trong phân tích thực phẩm và nước.
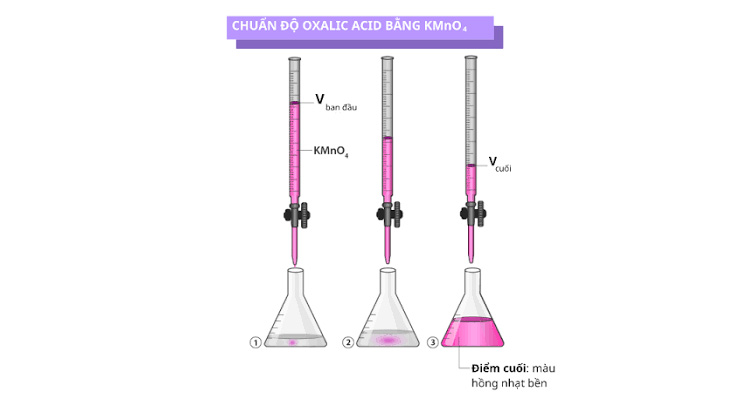
Thứ hai là titration oxy hóa – khử giúp xác định nồng độ các chất có khả năng trao đổi electron như Fe(3+) hay KMnO4. Tiếp đến là titration tạo phức dùng để định lượng ion kim loại bằng tác nhân tạo phức như EDTA và cuối cùng là titration kết tủa, dựa trên phản ứng tạo muối không tan, ví dụ titration Ag+ với Cl- bằng AgNO3. Ngoài ra, còn có titration Karl Fischer được dùng riêng để xác định hàm lượng nước trong mẫu.

Titration thêm dung dịch chuẩn vào mẫu đến khi phản ứng hoàn tất
Theo kỹ thuật, có titration trực tiếp (thêm dung dịch chuẩn vào mẫu đến khi phản ứng hoàn tất), titration ngược (thêm dư dung dịch chuẩn rồi chuẩn lại phần dư) và titration gián tiếp, áp dụng khi chất phân tích không thể titration trực tiếp. Khi thực hiện, việc nắm rõ phương trình chuẩn độ của phản ứng là rất quan trọng, vì nó giúp tính toán chính xác lượng chất chuẩn cần thiết dựa trên tỉ lệ mol giữa chất phân tích và dung dịch chuẩn.
Nguyên tắc hoạt động của phương pháp chuẩn độ trong hóa học
Phương pháp này trong hóa học hoạt động dựa trên nguyên tắc phản ứng hóa học giữa hai dung dịch, một dung dịch có nồng độ biết trước gọi là dung dịch chuẩn, và một dung dịch có nồng độ chưa biết là dung dịch cần phân tích. Trong quá trình titration, dung dịch chuẩn được thêm dần vào dung dịch cần phân tích cho đến khi phản ứng xảy ra hoàn toàn. Thể tích dung dịch chuẩn đã dùng chính là cơ sở để tính nồng độ của chất phân tích theo tỉ lệ phản ứng hóa học.
Một khái niệm quan trọng trong quá trình này là điểm tương đương, tức là thời điểm mà lượng dung dịch chuẩn vừa đủ để phản ứng hết với chất cần phân tích. Tuy nhiên, vì không thể quan sát trực tiếp điểm tương đương, người ta thường dựa vào điểm kết thúc, được nhận biết thông qua sự thay đổi của chất chỉ thị. Việc lựa chọn chất chỉ thị phù hợp giúp xác định chính xác khi nào phản ứng đã hoàn tất.
Ngoài ra, để kết quả của nó đạt độ chính xác cao, phản ứng giữa dung dịch chuẩn và dung dịch cần phân tích phải xảy ra nhanh, hoàn toàn và chọn lọc, không có phản ứng phụ làm sai lệch kết quả. Sau khi ghi nhận thể tích dung dịch chuẩn tiêu tốn, có thể áp dụng công thức chuẩn độ tính toán như C1V1 = C2V2 (với C là nồng độ, V là thể tích) để xác định nồng độ dung dịch chưa biết.
Hướng dẫn thao tác chuẩn độ đúng kỹ thuật cho người mới bắt đầu
Khi bắt đầu một phép titration, bước đầu tiên là chuẩn hóa dung dịch titration. Dung dịch chuẩn phải có nồng độ chính xác và ổn định để đảm bảo kết quả đáng tin cậy. Sau khi chuẩn hóa, mẫu cần phân tích được chuẩn bị: nếu là mẫu rắn cần hòa tan hoặc xử lý phù hợp, và nếu là dung dịch thì phải đảm bảo thể tích và điều kiện như pH thích hợp.

Hướng dẫn thao tác đúng kỹ thuật cho người mới
Tiếp theo, thao tác thực hiện titration yêu cầu dụng cụ chuẩn độ phải được xử lý và sử dụng đúng kỹ thuật. Tráng buret hoặc pipet bằng dung dịch cần phân tích hoặc dung dịch chuẩn để tránh sai số thể tích, đặt buret ở vị trí dễ đọc vạch và đảm bảo không có bọt khí. Khi thực hiện, dung dịch chuẩn được nhỏ từ từ vào mẫu có mặt chất chỉ thị hoặc thiết bị đo để xác định điểm kết thúc, đến khi xuất hiện màu sắc của chỉ thị hoặc tín hiệu đo thay đổi đột ngột thì dừng lại.
Cuối cùng, sau khi ghi lại thể tích dung dịch chuẩn đã tiêu tốn, cần thực hiện tính toán kết quả dựa vào tỷ lệ phản ứng, thể tích và nồng độ dung dịch chuẩn để xác định nồng độ của chất phân tích. Ngoài ra, để đảm bảo độ chính xác và tính tái lập cao, nên thực hiện phép đo nhắc lại ít nhất 2 – 3 lần và lấy giá trị trung bình, đồng thời kiểm soát các yếu tố ảnh hưởng như tốc độ nhỏ giọt, khuấy trộn dung dịch và lựa chọn chỉ thị phù hợp.
Chất chỉ thị trong chuẩn độ
Trong phép chuẩn độ, một thành phần không thể thiếu là chất chỉ thị, đó là hợp chất được thêm vào dung dịch để giúp xác định điểm kết thúc của phản ứng titration. Chất chỉ thị thường là axit hoặc bazơ yếu, có khả năng thay đổi màu sắc rõ rệt khi môi trường chuyển từ dạng này sang dạng khác (ví dụ thay đổi pH).

Chất chỉ thị là hợp chất quan trọng trong phản ứng titration
Vai trò chính của chất chỉ thị là báo hiệu khi lượng dung dịch chuẩn vừa đủ để phản ứng với chất phân tích (tức là khi đạt hoặc gần điểm tương đương). Khi phản ứng gần tới điểm tương đương, môi trường hóa học (như pH, điện thế, độ dẫn…) thay đổi nhanh; chất chỉ thị quan sát được sẽ đổi màu hoặc xuất hiện tín hiệu giúp người làm thí nghiệm dừng lại đúng lúc.
Việc lựa chọn chất chỉ thị phù hợp rất quan trọng. Khoảng pH chuyển màu của chỉ thị phải nằm gần với pH của điểm tương đương của phản ứng titration, màu sắc chuyển rõ ràng và chất chỉ thị đó không ảnh hưởng tới phản ứng chính.
Ứng dụng của chuẩn độ trong thực tế
Phép chuẩn độ nhờ vào tính chính xác, độ nhạy và khả năng chọn lọc cao, đã được ứng dụng rộng rãi trong rất nhiều lĩnh vực thực tế. Trong ngành công nghiệp thực phẩm & đồ uống, nó thường được sử dụng để xác định hàm lượng axit, độ chua, salt hoặc các ion kim loại trong sản phẩm nhằm đảm bảo hương vị, độ an toàn và tuổi thọ sản phẩm.
Trong lĩnh vực môi trường và quản lý nguồn nước, thí nghiệm chuẩn độ góp phần đo đạc các thông số quan trọng như pH, độ kiềm, nồng độ ion kim loại nặng hoặc chất ô nhiễm trong nước thải và môi trường, từ đó hỗ trợ việc đánh giá mức độ ô nhiễm và thiết kế quy trình xử lý phù hợp. Còn trong ngành dược phẩm và hóa chất, phương pháp này được sử dụng để xác định đúng nồng độ hoạt chất trong thuốc, kiểm soát độ tinh khiết của nguyên liệu và đảm bảo đáp ứng tiêu chuẩn chất lượng trước khi đưa ra thị trường.
Có thể thấy, chuẩn độ không chỉ là phương pháp cơ bản trong hóa học phân tích mà còn là công cụ quan trọng trong đời sống và sản xuất. Việc hiểu rõ nguyên tắc, thao tác và lựa chọn chất chỉ thị phù hợp sẽ đảm bảo kết quả phân tích hiệu quả và ứng dụng thực tế tối ưu.


