Axit sunfuric đóng vai trò then chốt trong nhiều ngành công nghiệp. Từ sản xuất phân bón, chế tạo ắc quy đến xử lý nước thải, H2SO4 đều có ứng dụng quan trọng. Tuy nhiên, sử dụng H2SO4 tiềm ẩn nhiều nguy hiểm. Cẩm nang sau cung cấp cho bạn kiến thức toàn diện về axit này, từ tính chất, ứng dụng, cách sử dụng an toàn. Đọc ngay để tìm hiểu chi tiết.
Giới thiệu chung về Axit Sunfuric (H2SO4)
Sunfuric Axit được mệnh danh là vua của các loại hóa chất. Vậy Axit Sunfuric là gì? Axit Sunfuric là chất gì mà lại có sức ảnh hưởng lớn đến vậy?

H2SO4 là vua của các loại hóa chất
H2SO4 là một axit vô cơ mạnh tồn tại ở dạng lỏng không màu, không mùi vị và không bay hơi. Đặc biệt, nó nặng hơn nước và có khả năng tan vào không khí ở bất kỳ nồng độ nào. Chính những đặc tính này đã góp phần làm nên ngai vàng của H2SO4 trong thế giới hóa học.
Bạn có biết? Sunfuric Axit thậm chí còn có trong nước mưa. Cảm giác ngứa ngáy, khó chịu khi dính nước mưa chính là do tác dụng của H2SO4 loãng đấy.
Đặc điểm kỹ thuật
Để hiểu rõ hơn về H2SO4, chúng ta cùng phân tích những đặc điểm kỹ thuật, quyết định tính chất và ứng dụng của nó trong thực tiễn.
- Công thức hóa học của axit sunfuric: H2SO4
- Khối lượng mol: 98.079 g/mol
- Tỷ trọng: 1.84 g/cm³
- Điểm nóng chảy: 10.38 °C
- Điểm sôi: 337 °C
- Độ nhớt: 26.7 cP ở 25 °C
Các tính chất cơ bản của H2SO4
Tính chất vật lý
- Dung dịch axit sunfuric là một chất lỏng sánh, không màu, có khối lượng riêng gần gấp đôi nước.
- Một đặc tính nổi bật của axit này là khả năng hút ẩm mạnh, nó có thể hút nước từ không khí và thậm chí là từ các hợp chất hữu cơ.
- Khi tan trong nước, H2SO4 tỏa ra một lượng nhiệt lớn.
- Nhiều người thắc mắc “Axit sunfuric có bay hơi không?”. Câu trả lời là có, tuy nhiên do có điểm sôi cao nên nó bay hơi rất chậm.
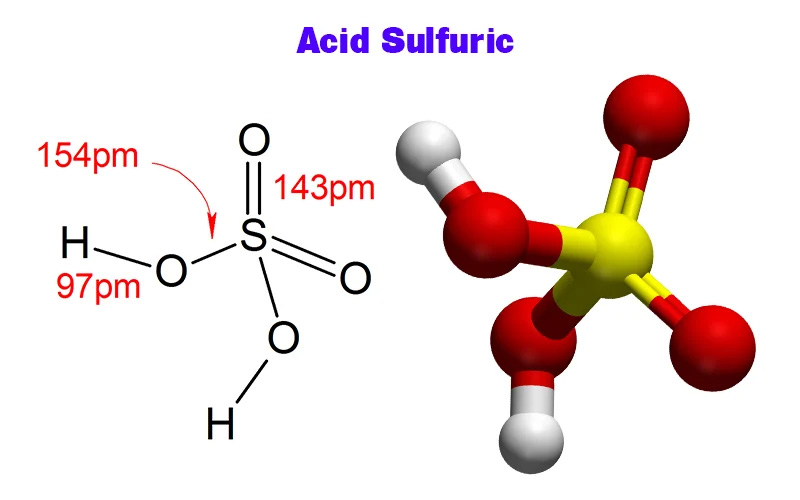
Cấu trúc hóa học của H2SO4
Tính chất hóa học của Axit Sunfuric
Mặc dù đều được gọi là sunfuric axit, nhưng thực tế có hai loại với những đặc tính hóa học riêng biệt: H2SO4 loãng và H2SO4 đặc.
H2SO4 loãng mang đầy đủ tính chất của một axit mạnh thông thường. Nó làm quỳ tím chuyển đỏ, phản ứng với kim loại, bazơ, oxit bazơ và muối để tạo ra các hợp chất mới.
Axit sunfuric đặc không chỉ sở hữu các tính chất của axit loãng mà còn có những điểm khác biệt đáng chú ý. Ví dụ, khi phản ứng với sắt, nếu thêm đồng (Cu) vào dung dịch, ta sẽ quan sát thấy màu xanh đặc trưng.
Đặc biệt, H2SO4 đặc còn thể hiện tính háo nước mạnh mẽ. Một minh chứng rõ ràng là khi cho H2SO4 đặc vào chén nước, chỉ sau vài phút, nước sẽ chuyển sang màu đen và sủi bọt dữ dội do axit hút nước từ các hợp chất hữu cơ.
Các quy trình sản xuất H2SO4
Sản xuất axit sunfuric chủ yếu bằng quy trình tiếp xúc gồm ba giai đoạn:
- Oxi hóa SO2 thành sulfur trioxide (SO3): Sử dụng chất xúc tác
- Sản xuất sulfur dioxide (SO2): Đốt cháy lưu huỳnh hoặc quặng sunfua.
- vanadi pentoxit (V2O5).
- Hấp thụ SO3 vào H2SO4 đặc: Tạo thành oleum (H2S2O7), sau đó pha loãng với nước.
H2SO4 và các ứng dụng thực tiễn
Được mệnh danh là “vua hóa chất”, ứng dụng của Axit Sunfuric trải rộng trên nhiều lĩnh vực của đời sống, đặc biệt là trong các ngành công nghiệp quan trọng.
Trong công nghiệp
Trong lĩnh vực công nghiệp, H2SO4 đóng vai trò then chốt và được ứng dụng rộng rãi trong nhiều quy trình sản xuất. Một trong những ứng dụng quan trọng nhất là sản xuất phân bón, đặc biệt là phân lân và phân amoni sunfat, giúp cung cấp dinh dưỡng cho cây trồng.
Bên cạnh đó, H2SO4 còn được sử dụng trong sản xuất nhiều loại hóa chất khác nhau, bao gồm các axit khác, chất tẩy rửa, thuốc nhuộm… Trong ngành luyện kim, nó được dùng để tẩy gỉ và làm sạch bề mặt kim loại trước khi gia công, góp phần nâng cao chất lượng sản phẩm.
Trong phòng thí nghiệm
Trong phòng thí nghiệm, H2SO4 là một hóa chất quen thuộc với các nhà khoa học. Với tính chất hóa học đặc trưng, axit này được sử dụng rộng rãi như một loại thuốc thử quan trọng trong nhiều phản ứng hóa học.
Nó tham gia vào các phản ứng với kim loại, oxit kim loại, bazơ để tạo ra muối sunfat, cũng như được sử dụng trong các phản ứng oxi hóa khử. Ngoài ra, sunfuric axit còn đóng vai trò là chất xúc tác trong nhiều phản ứng hữu cơ, giúp tăng tốc độ phản ứng và nâng cao hiệu suất tổng hợp các hợp chất hữu cơ.
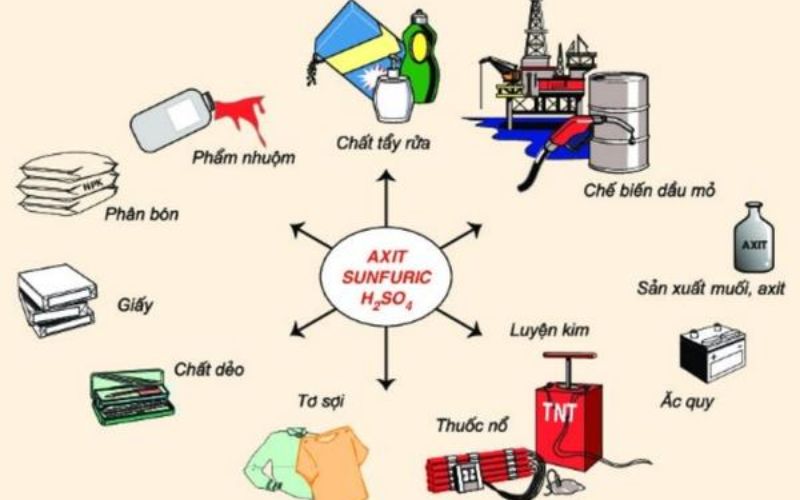
H2SO4 là axit có đa dạng ứng dụng trong cuộc sống
Xử lý nước thải
Trong lĩnh vực xử lý nước thải, H2SO4 là một hóa chất quan trọng giúp cải thiện chất lượng nước và bảo vệ môi trường. Với tính axit mạnh, H2SO4 được sử dụng để điều chỉnh độ pH của nước thải, trung hòa nước thải có tính kiềm, đưa pH về mức an toàn cho phép trước khi thải ra môi trường.
Ngoài ra, nó còn có khả năng loại bỏ các chất ô nhiễm trong nước thải, bao gồm kết tủa các ion kim loại nặng, loại bỏ các chất hữu cơ độc hại, góp phần làm sạch nguồn nước và giảm thiểu ô nhiễm môi trường.
Ứng dụng khác
Bên cạnh những ứng dụng kể trên, sunfuric axit còn đóng góp vai trò quan trọng trong nhiều lĩnh vực khác. Trong ngành dầu mỏ, H2SO4 được sử dụng trong quá trình lọc dầu và tinh chế các sản phẩm dầu mỏ, giúp nâng cao chất lượng nhiên liệu.
Ngoài ra, nó còn được ứng dụng rộng rãi trong sản xuất ắc quy chì-axit cho các phương tiện giao thông và thiết bị điện. H2SO4 trong ắc quy đóng vai trò là chất điện li, tạo điều kiện cho các phản ứng hóa học xảy ra và tạo ra dòng điện.
Hướng dẫn sử dụng an toàn và bảo quản H2SO4
Axit sunfuric có độc không? Câu trả lời là CÓ. Những tác hại của axit sunfuric loãng có thể kể đến như kích ứng da, mắt, đường hô hấp. Trong khi đó, dung dịch H2SO4 đặc có thể gây bỏng nặng, làm hỏng giác mạc, dẫn đến mù lòa. Nuốt phải axit này sẽ đau đớn dữ dội, nôn mửa, chảy máu nội tạng và thậm chí tử vong. Vì vậy, việc tuân thủ nghiêm ngặt các quy định an toàn khi sử dụng và bảo quản là vô cùng quan trọng.
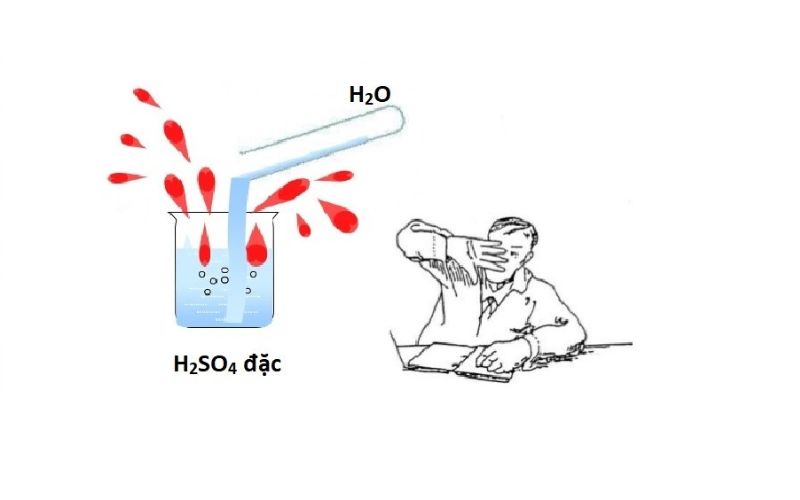
Tuyệt đối không được đổ trực tiếp nước vào dung dịch H2SO4 đặc
Để đảm bảo an toàn khi tiếp xúc với dung dịch H2SO4 , bạn cần:
- Sử dụng đầy đủ các trang bị bảo hộ lao động như găng tay, kính và khẩu trang… khi tiếp xúc với H2SO4
- Pha loãng axit: Luôn luôn cho từ từ axit vào nước.
- Bảo quản: Để H2SO4 ở nơi khô ráo, thoáng mát và tránh ánh nắng trực tiếp từ mặt trời.
Bị dính H2SO4 phải làm sao?
- Trên da: Rửa ngay vùng da bị dính axit với nhiều nước sạch trong ít nhất 20 phút. Sau đó, dùng dung dịch NaHCO3 1% để trung hòa axit còn sót lại.
- Vào mắt: Rửa mắt với nước sạch trong ít nhất 15 phút, sau đó đến cơ sở y tế gần nhất để được kiểm tra.
- Hít phải: Di chuyển đến nơi thoáng khí ngay lập tức. Nếu có triệu chứng khó thở, hãy đến bệnh viện ngay.
- Nuốt phải: TUYỆT ĐỐI KHÔNG cố gây nôn. Hãy uống nhiều nước hoặc sữa và đến bệnh viện ngay lập tức.
Quy định quản lý và xử phạt khi vi phạm về H2SO4
H2SO4 tuy quan trọng nhưng cũng rất nguy hiểm, nên việc sản xuất, kinh doanh, vận chuyển và sử dụng nó được quản lý chặt chẽ bởi Luật Hóa chất và Nghị định 113/2017/NĐ-CP.
Cụ thể, cần có giấy phép, điều kiện sản xuất, kinh doanh, vận chuyển, bảo quản… đúng quy định. Việc sử dụng phải đảm bảo an toàn lao động và bảo vệ môi trường. Tùy theo mức độ vi phạm, các hình thức xử lý có thể bao gồm từ xử phạt hành chính (như cảnh cáo, phạt tiền, tịch thu…) đến truy cứu trách nhiệm hình sự.
Hanimex – Đơn vị cung cấp H2SO4 uy tín tại Hà Nội
Bạn đang tìm kiếm địa chỉ uy tín để mua axit sunfuric chất lượng? Hanimex chính là sự lựa chọn hoàn hảo dành cho bạn!

Liên hệ với Hanimex để mua H2SO4 với giá tốt nhất
Tại sao nên chọn Hanimex?
- Chất lượng hàng đầu: Hanimex chuyên cung cấp H2SO4 chất lượng cao, đáp ứng đa dạng nhu cầu sử dụng, kể cả mua bán lẻ axit sunfuric tại Hà Nội.
- Giá cả cạnh tranh: Công ty cam kết mang đến giá axit sunfuric tốt nhất trên thị trường.
- Tư vấn tận tâm: Đội ngũ chuyên viên giàu kinh nghiệm sẵn sàng tư vấn mọi thắc mắc của bạn.
- Giao hàng nhanh chóng: Dịch vụ giao hàng chuyên nghiệp, đảm bảo sản phẩm đến tay bạn nhanh nhất.
Liên hệ ngay với Hanimex để được tư vấn và báo giá chi tiết!









Bảo Ngọc –
Sản phẩm dễ bảo quản, đóng hàng chắc chắn, không bị rò rỉ.