Khám phá cách các nguyên tử gắn kết với nhau qua liên kết cộng hóa trị chính là chìa khóa mở ra bí mật của thế giới hóa học đa sắc màu. Hình thức liên kết này không chỉ tạo nên những phân tử bền vững mà còn là nền tảng cho vô vàn hiện tượng tự nhiên và công nghệ tiên tiến ngày nay. Hãy cùng tìm hiểu để hiểu rõ hơn về sức mạnh kết nối tuyệt vời này.
Liên kết cộng hóa trị là gì?
Khi hai nguyên tử cùng chia sẻ electron để đạt được sự ổn định, một kiểu tương tác đặc biệt sẽ hình thành, đóng vai trò then chốt trong việc gắn kết các nguyên tử thành phân tử. Trong quá trình này, các cặp electron dùng chung chính là yếu tố tạo nên sự liên kết, trong khi những electron không tham gia sẽ tồn tại như các cặp đơn độc. Chính sự chia sẻ này giúp nguyên tử tiến gần đến cấu hình electron của khí hiếm, từ đó tạo ra các hợp chất bền vững trong tự nhiên. Việc hiểu rõ khái niệm liên kết cộng hóa trị là chìa khóa để giải thích cách các chất hình thành và tồn tại ở cấp độ vi mô.

Đây là loại liên kết được hình thành khi hai nguyên tử cùng chia sẻ electron để đạt được sự ổn định cấu hình.
Bản chất của liên kết cộng hóa trị và vai trò trong hóa học
Trong thế giới vi mô, khi các nguyên tử có độ âm điện tương đương tiến lại gần nhau và cùng chia sẻ electron, một kiểu gắn kết bền vững sẽ được hình thành. Sự chia sẻ này có thể diễn ra với một, hai hoặc ba cặp electron, tùy thuộc vào mức độ tương tác giữa các nguyên tử. Chính cơ chế đó tạo nền tảng cho nhiều phân tử trong tự nhiên, từ các hợp chất vô cơ đơn giản đến những hợp chất hữu cơ phức tạp. Việc hiểu rõ tính chất của liên kết cộng hóa trị không chỉ giúp lý giải cấu trúc phân tử mà còn làm sáng tỏ nhiều hiện tượng và phản ứng quan trọng trong hóa học.
Cách hình thành liên kết cộng hóa trị giữa các nguyên tử
Khi hai nguyên tử cùng chia sẻ electron từ lớp vỏ ngoài, chúng tạo nên một liên kết giúp cả hai đạt được trạng thái ổn định hơn về mặt cấu hình electron. Liên kết cộng hóa trị được hình thành do chính quá trình chia sẻ này, trong đó mỗi nguyên tử góp phần tạo ra một hoặc nhiều cặp electron dùng chung.
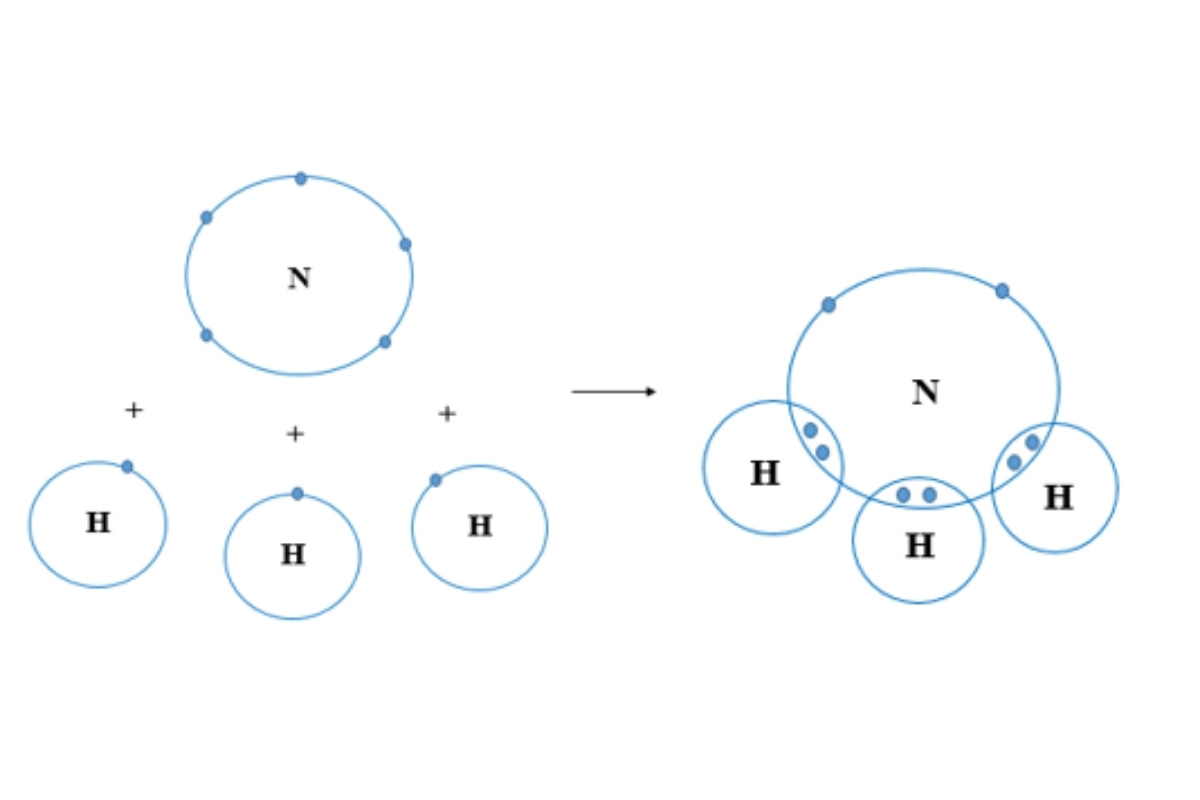
Khi hai nguyên tử cùng chia sẻ electron chúng tạo nên một liên kết giúp cả hai đạt được trạng thái ổn định hơn về mặt cấu hình electron.
Tùy vào số lượng electron được chia sẻ, liên kết có thể là đơn, đôi hoặc ba, như trường hợp phân tử hydro (H₂) với một cặp electron, hay phân tử nitơ (N₂) với ba cặp electron liên kết.
Sự hình thành liên kết cộng hóa trị mang tính chọn lọc, phụ thuộc vào khả năng hút electron của các nguyên tử tham gia. Thường thì liên kết cộng hóa trị thường được hình thành giữa các nguyên tử phi kim có độ âm điện tương đương hoặc gần nhau, tạo nên sự cân bằng trong lực hút và sự ổn định của phân tử.
Phân biệt liên kết cộng hóa trị có cực và không cực
Khi hai nguyên tử chia sẻ electron để tạo thành phân tử, mức độ chênh lệch về độ âm điện giữa chúng sẽ quyết định tính phân cực của liên kết. Nếu hai nguyên tử có độ âm điện gần như bằng nhau, cặp electron dùng chung sẽ được phân bố đều, tạo nên sự cân bằng trong phân tử. Trường hợp này thường xảy ra giữa các nguyên tử cùng loại, chẳng hạn như trong các phân tử H₂, O₂ hay N₂ – đây là những ví dụ về liên kết cộng hóa trị không phân cực tiêu biểu.
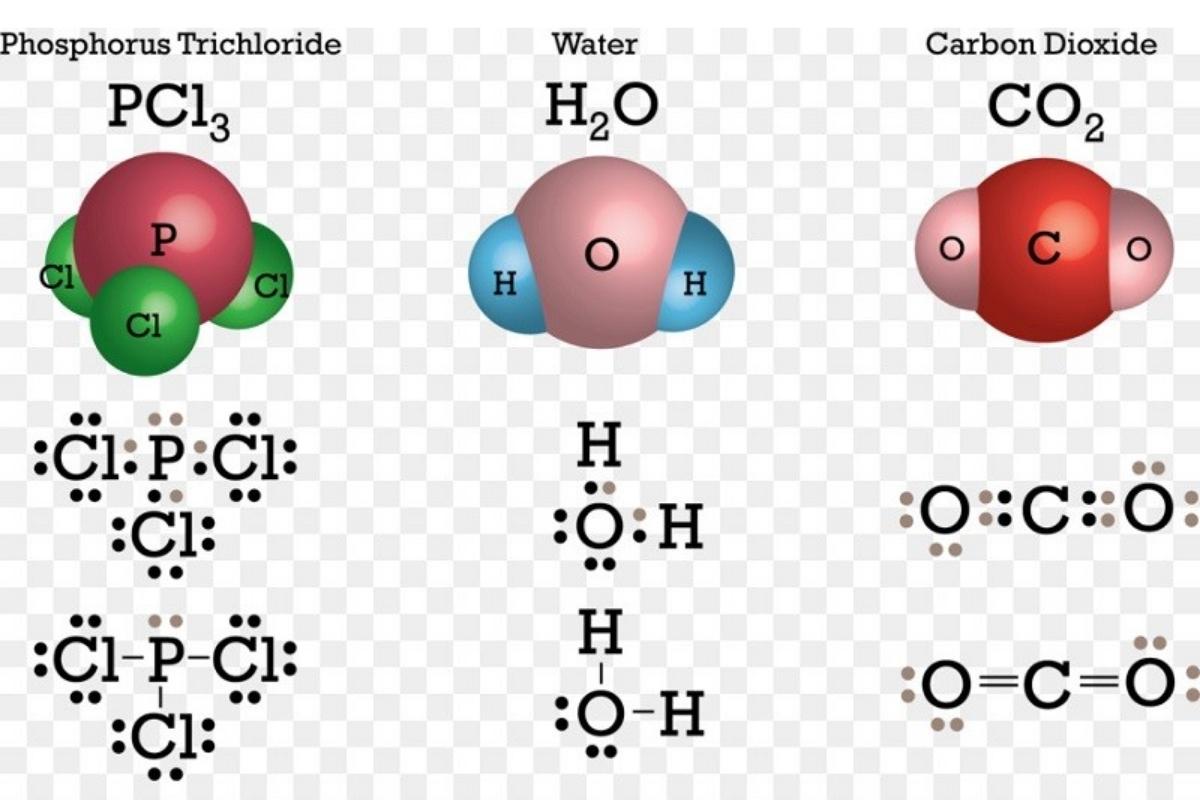
Căn cứ vào mức độ chênh lệch về độ âm điện giữa chúng sẽ quyết định tính phân cực của liên kết.
Ngược lại, khi độ âm điện giữa hai nguyên tử khác nhau đáng kể, cặp electron sẽ bị lệch về phía nguyên tử có xu hướng hút electron mạnh hơn. Điều này tạo ra sự phân bố không đồng đều về mật độ điện tích, làm cho phân tử trở nên phân cực – như trong phân tử HCl, nơi electron nghiêng về phía clo. Mức độ phân cực này phản ánh qua hiệu độ âm điện giữa hai nguyên tử, và nếu sự chênh lệch vượt ngưỡng nhất định, liên kết sẽ mang đặc điểm hoàn toàn khác như trong trường hợp liên kết ion.
Bảng phân loại liên kết dựa trên hiệu độ âm điện:
| Hiệu độ âm điện (ΔEN) | Loại liên kết |
| 0,0 ≤ ΔEN < 0,4 | Liên kết cộng hóa trị không cực |
| 0,4 ≤ ΔEN < 1,7 | Liên kết cộng hóa trị có cực |
| ΔEN ≥ 1,7 | Liên kết ion |
Liên kết cộng hóa trị xuất hiện ở đâu trong đời sống hằng ngày?
Trong đời sống hằng ngày, kiểu liên kết giữa các nguyên tử để tạo thành phân tử ổn định xuất hiện rất phổ biến. Một ví dụ điển hình là nước – hợp chất không thể thiếu cho sự sống. Trong phân tử nước, các nguyên tử hydro và oxy chia sẻ electron với nhau, tạo nên một mối liên kết bền vững. Chính điều này giúp nước có những tính chất đặc biệt như khả năng hòa tan cao và điểm sôi cao hơn nhiều so với các chất có khối lượng tương đương.
Không khí mà chúng ta hít thở mỗi ngày cũng là một minh chứng. Các phân tử oxy (O₂) và nitơ (N₂) đều được hình thành từ hai nguyên tử giống nhau gắn kết bằng cách chia sẻ electron, tạo nên những phân tử khí ổn định và chiếm phần lớn thành phần khí quyển.
Kiểu liên kết giữa các nguyên tử để tạo thành phân tử ổn định xuất hiện rất phổ biến trong cuộc sống.
Ngoài ra, trong các hợp chất hữu cơ quen thuộc như metan (CH₄) hay etanol (C₂H₅OH), các nguyên tử cacbon, hydro và oxy cũng kết hợp với nhau thông qua cách thức tương tự. Những mối liên kết này là nền tảng để tạo nên các vật liệu, nhiên liệu và hợp chất thiết yếu phục vụ đời sống con người.
Tầm quan trọng của liên kết cộng hóa trị trong sinh học và công nghiệp
Trong sinh học, mối gắn kết giữa các nguyên tử trong phân tử chính là nền tảng tạo nên cấu trúc và chức năng của những hợp chất thiết yếu như ADN, protein, carbohydrate hay lipid. Nhờ sự chia sẻ electron giữa các nguyên tử, các phân tử sinh học này có được sự ổn định cần thiết để thực hiện các chức năng phức tạp trong cơ thể sống. Ví dụ, cấu trúc bền vững của ADN hay độ chính xác trong cách gập cuộn của protein đều phụ thuộc vào kiểu liên kết này giữa các nguyên tử cacbon, hydro, oxy và nitơ.
Trong lĩnh vực công nghiệp, việc nắm vững cách các nguyên tử liên kết với nhau đóng vai trò quan trọng trong nghiên cứu và sản xuất. Từ dược phẩm đến vật liệu tổng hợp hay hóa chất chuyên dụng, khả năng thiết kế các hợp chất với cấu trúc chính xác và tính chất mong muốn dựa trên sự hiểu biết về loại liên kết này giúp các nhà khoa học tạo ra những sản phẩm vừa hiệu quả vừa thân thiện với môi trường. Điều đó cho thấy, kiểu liên kết giữa các nguyên tử không chỉ giữ vai trò trung tâm trong thế giới sinh học mà còn là công cụ thiết yếu cho đổi mới công nghệ và phát triển bền vững.
Hiểu được cách nguyên tử hợp tác qua liên kết cộng hóa trị giúp ta giải mã cấu trúc và tính năng của vô số hợp chất quan trọng. Đây chính là nền tảng cho các bước tiến đột phá trong khoa học và ứng dụng thực tiễn, từ y học đến công nghiệp, mở rộng giới hạn sáng tạo và khám phá thế giới xung quanh ta.


