Bazơ là nhóm chất giữ vai trò then chốt trong nhiều phản ứng hóa học và ứng dụng thực tiễn. Không chỉ giúp cân bằng độ pH trong môi trường, bazơ còn góp mặt trong các ngành như công nghiệp, y học và xử lý nước. Sự đa dạng trong tính chất và khả năng phản ứng khiến chúng trở thành thành phần không thể thiếu trong đời sống hằng ngày!
Bazơ là gì?
Định nghĩa Bazơ là một nhóm hợp chất hóa học giữ vai trò quan trọng trong nhiều phản ứng và quá trình tự nhiên. Trong cấu trúc phân tử của chúng, thường xuất hiện một nguyên tử kim loại kết hợp với một hoặc nhiều nhóm hydroxyl (OH), còn gọi là hidroxit. Khi hòa tan trong nước, những hợp chất này tạo ra dung dịch có độ pH lớn hơn 7, thể hiện rõ tính kiềm. Chúng có khả năng nhận proton (H⁺) hoặc giải phóng ion hydroxyl (OH⁻), khiến môi trường trở nên bazơ hơn và làm đổi màu giấy quỳ tím sang xanh.

Cấu trúc phân tử của chúng có chứa một hay nhiều nhóm hydroxyl (OH)
Một số chất dù không tan trong nước vẫn thể hiện tính chất này khi phản ứng với axit hoặc các hợp chất khác. Trong hóa học, khái niệm bazơ được dùng để chỉ chung cho các chất có những đặc điểm nói trên, kể cả ở dạng tan hay không tan, tùy theo ngữ cảnh phản ứng cụ thể.
Tính chất hóa học đặc trưng của bazơ
Bazơ là chất gì mà có thể tham gia vào nhiều phản ứng đặc trưng của hóa học? Những hợp chất này thường thể hiện rõ nét qua tính chất hóa học của bazơ, như khả năng làm quỳ tím chuyển xanh hay phenolphthalein đổi sang đỏ hồng trong dung dịch.
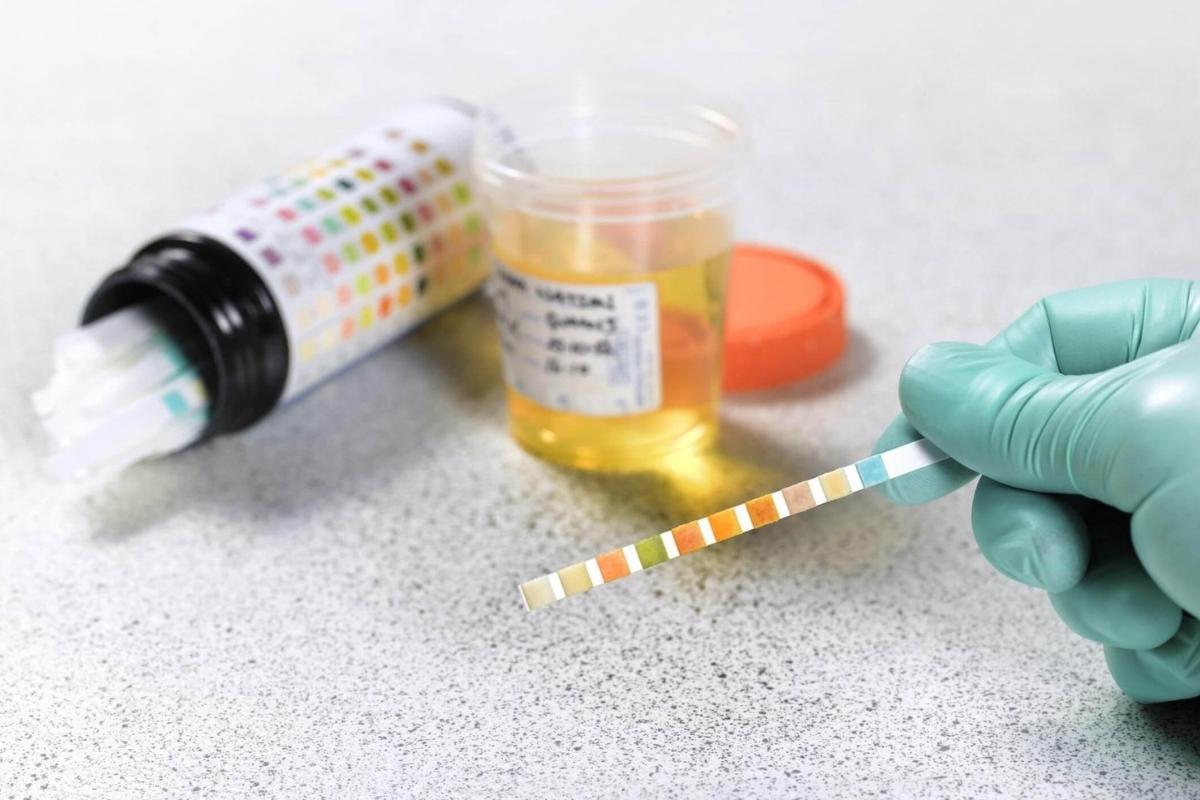
Đây là chất có thể tham gia được nhiều phản ứng đặc trưng trong hóa học
Chúng phản ứng với axit để tạo thành muối và nước, ví dụ:
KOH + HCl → KCl + H₂O
Khi tác dụng với oxit axit, chúng cũng tạo ra muối và nước:
2NaOH + SO₂ → Na₂SO₃ + H₂O
Một số phản ứng trao đổi còn xảy ra giữa dung dịch kiềm và muối, trong đó có thể tạo kết tủa:
2NaOH + CuSO₄ → Na₂SO₄ + Cu(OH)₂↓
Với những bazơ không tan, nhiệt độ cao có thể khiến chúng phân hủy, như:
Cu(OH)₂ → CuO + H₂O
Trong số đó, NaOH và KOH là đại diện cho nhóm bazơ mạnh nhất, dễ tan và phản ứng nhanh, trong khi các bazơ yếu như Mg(OH)₂ lại tan kém và phản ứng chậm hơn, thường chỉ hoạt động rõ trong một số điều kiện nhất định.
So sánh các loại bazơ phổ biến
Dưới đây là bảng so sánh các loại hợp chất kiềm phổ biến, được phân loại dựa trên tính tan và đặc điểm hóa học:
| Loại | Tính tan trong nước | Ví dụ điển hình | Tính chất hóa học | Ghi chú |
| Kiềm mạnh | Tan hoàn toàn | NaOH (natri hidroxit), KOH (kali hidroxit), LiOH | Phản ứng yếu, dễ phân hủy khi đun nóng | Tạo dung dịch có pH cao, tính kiềm mạnh |
| Kiềm yếu | Không tan hoặc tan ít | Al(OH)3, Fe(OH)3, Cu(OH)2 | Phản ứng yếu, dễ phân hủy khi đun nóng | Thường tạo kết tủa trong phản ứng |
| Kiềm tan (kiềm kiềm thổ) | Tan tốt | Ca(OH)2 (vôi tôi), Ba(OH)2 | Tạo dung dịch kiềm, phản ứng với axit và muối | Ca(OH)2 tan ít, ứng dụng trong xây dựng |
| Kiềm không tan | Không tan | Mg(OH)2, Fe(OH)3, Cu(OH)2 | Phân hủy khi đun nóng, tạo oxit và nước | Dùng trong xử lý nước và làm thuốc |
Ứng dụng thực tế của bazơ trong công nghiệp và đời sống
Bazơ là nhóm hợp chất có vai trò thiết yếu trong nhiều lĩnh vực nhờ khả năng tạo môi trường kiềm và tham gia vào các phản ứng hóa học quan trọng. Dưới đây là một số ứng dụng phổ biến và có ảnh hưởng sâu rộng trong thực tế:

Sản xuất xà phòng, chất tẩy rửa là ứng dụng dễ thấy nhất
Xử lý nước: Trong xử lý nước thải và nước sinh hoạt, các ví dụ về bazơ như NaOH hoặc Ca(OH)₂ được dùng để điều chỉnh pH, trung hòa axit và kết tủa các kim loại nặng. Điều này không chỉ giúp làm sạch nguồn nước mà còn bảo vệ đường ống, thiết bị xử lý khỏi bị ăn mòn.
Sản xuất xà phòng và chất tẩy rửa: NaOH là nguyên liệu chủ chốt trong quá trình xà phòng hóa – phản ứng giữa chất béo và kiềm để tạo thành muối natri của axit béo. Nhờ phản ứng này, các sản phẩm như xà phòng, nước rửa chén và bột giặt được tạo ra với khả năng làm sạch cao.
Ngành dệt nhuộm: Trước khi nhuộm vải, kiềm được dùng để xử lý bề mặt sợi, giúp vải mềm và tăng khả năng hấp thụ màu. Nhờ đó, màu sắc của sản phẩm đồng đều, bền đẹp hơn, đồng thời nâng cao chất lượng và giá trị hàng dệt may.
Xây dựng: Vôi tôi – một dạng bazơ phổ biến – được sử dụng để trộn vữa và cải thiện độ kết dính của vật liệu xây dựng. Ngoài ra, nhờ tính kháng khuẩn nhẹ, nó còn được dùng để khử trùng nền đất và môi trường xây dựng.
Phòng thí nghiệm và nghiên cứu: Trong phân tích hóa học, kiềm thường được dùng để trung hòa axit, điều chỉnh môi trường phản ứng hoặc làm thuốc thử kiểm tra chất chỉ thị. Đây là thành phần không thể thiếu trong các thí nghiệm định tính, định lượng.
Dù hiện diện âm thầm trong nhiều quá trình, các hợp chất bazơ đóng vai trò nền tảng trong cả công nghiệp lẫn đời sống hằng ngày. Việc hiểu và sử dụng đúng chúng góp phần nâng cao hiệu quả sản xuất và bảo vệ môi trường.
Cách điều chế bazơ trong phòng thí nghiệm

Cách điều chế trong phòng thí nghiệm
Trong phòng thí nghiệm, việc điều chế các hợp chất có tính kiềm thường được thực hiện bằng nhiều phương pháp khác nhau, tùy thuộc vào tính chất của chất cần thu. Một cách phổ biến là cho kim loại kiềm hoặc kiềm thổ phản ứng trực tiếp với nước, tạo ra dung dịch kiềm cùng với khí hidro, chẳng hạn:
2Na + 2H₂O → 2NaOH + H₂↑
Ngoài ra, một số oxit kim loại tan cũng có thể tác dụng với nước để tạo thành dung dịch kiềm, như trong phản ứng:
CaO + H₂O → Ca(OH)₂
Trong những trường hợp khác, dung dịch kiềm có thể được tạo ra bằng cách trung hòa axit bằng lượng kiềm dư, thu được muối và phần kiềm còn lại sau phản ứng.
Đối với những hợp chất không tan trong nước, người ta thường điều chế bằng phản ứng kết tủa. Ví dụ, khi trộn dung dịch muối đồng sunfat với dung dịch natri hydroxide, sẽ thu được kết tủa màu xanh lam:
CuSO₄ + 2NaOH → Cu(OH)₂↓ + Na₂SO₄
Tùy vào mục đích sử dụng và tính chất của chất cần thu, mỗi phương pháp đều có thể được lựa chọn sao cho phù hợp và hiệu quả trong thực tiễn nghiên cứu và giảng dạy.
Tìm hiểu vai trò của bazơ trong phản ứng trao đổi ion
Trong các phản ứng trao đổi ion, bazơ đóng vai trò quan trọng khi tan trong nước và phân li thành ion hydroxyl (OH⁻) cùng ion kim loại. Ion OH⁻ dễ dàng tham gia phản ứng với các ion khác trong dung dịch, tạo ra các hợp chất mới hoặc kết tủa.
Khi dung dịch bazơ phản ứng với muối, nó có thể đẩy ion kim loại yếu hơn ra khỏi muối, tạo thành muối mới và hydroxide của kim loại đó. Quá trình này rất hữu ích trong xử lý nước và tách kim loại khỏi dung dịch.
Ngoài ra, bazơ còn giúp điều chỉnh độ pH của dung dịch, từ đó ảnh hưởng đến cân bằng ion trong nhiều quy trình công nghiệp cũng như xử lý môi trường.
Nhóm hợp chất kiềm rất đa dạng về tính chất và giữ vai trò quan trọng trong nhiều lĩnh vực khác nhau. Việc nắm vững kiến thức về bazơ giúp chúng ta ứng dụng hiệu quả hơn trong công nghiệp và nghiên cứu khoa học. Hy vọng qua bài viết, bạn đã có cái nhìn tổng quan và sâu sắc hơn về vai trò thiết yếu của những chất này trong cuộc sống hàng ngày.


