Trong thế giới hóa học, các liên kết giữa ion đóng vai trò quan trọng trong việc tạo nên nhiều chất có tính chất đặc biệt. Những hợp chất này không chỉ góp mặt trong phòng thí nghiệm mà còn hiện diện khắp nơi trong cuộc sống hàng ngày, từ thực phẩm đến công nghiệp. Hiểu rõ về cấu tạo và tính chất của chúng giúp ta ứng dụng hiệu quả hơn trong nhiều lĩnh vực.
Hợp chất ion là gì?
Các chất được tạo thành từ sự kết hợp giữa các ion mang điện tích trái dấu – tức ion dương (cation) và ion âm (anion) – chính là một dạng hợp chất phổ biến trong hóa học. Thông thường, cation là những ion kim loại như natri (Na⁺), canxi (Ca²⁺) hay nhôm (Al³⁺), còn anion có thể là các ion phi kim hoặc các gốc axit như clorua (Cl⁻), sunfat (SO₄²⁻) hay nitrat (NO₃⁻).
Là sự kết hợp giữa các ion mang điện tích trái dấu.
Khi các ion này liên kết với nhau thông qua lực hút tĩnh điện mạnh, chúng tạo nên cấu trúc mạng tinh thể bền vững. Chính cấu trúc này là nền tảng để hầu hết các hợp chất ion thể hiện những tính chất đặc trưng như điểm nóng chảy cao, khả năng dẫn điện khi hòa tan trong nước hoặc ở trạng thái nóng chảy.
Tìm hiểu về liên kết ion và cách hình thành hợp chất ion
Liên kết ion là một dạng liên kết hóa học hình thành khi nguyên tử kim loại và phi kim tham gia trao đổi electron với nhau. Trong quá trình này, nguyên tử kim loại mất electron và trở thành ion dương (cation), trong khi nguyên tử phi kim nhận electron để trở thành ion âm (anion). Sự khác biệt đáng kể về độ âm điện – thường từ 1,7 trở lên – giữa hai nguyên tử chính là yếu tố thúc đẩy sự hình thành liên kết này. Các ion trái dấu sau đó hút nhau nhờ lực tĩnh điện, tạo nên một cấu trúc ổn định.
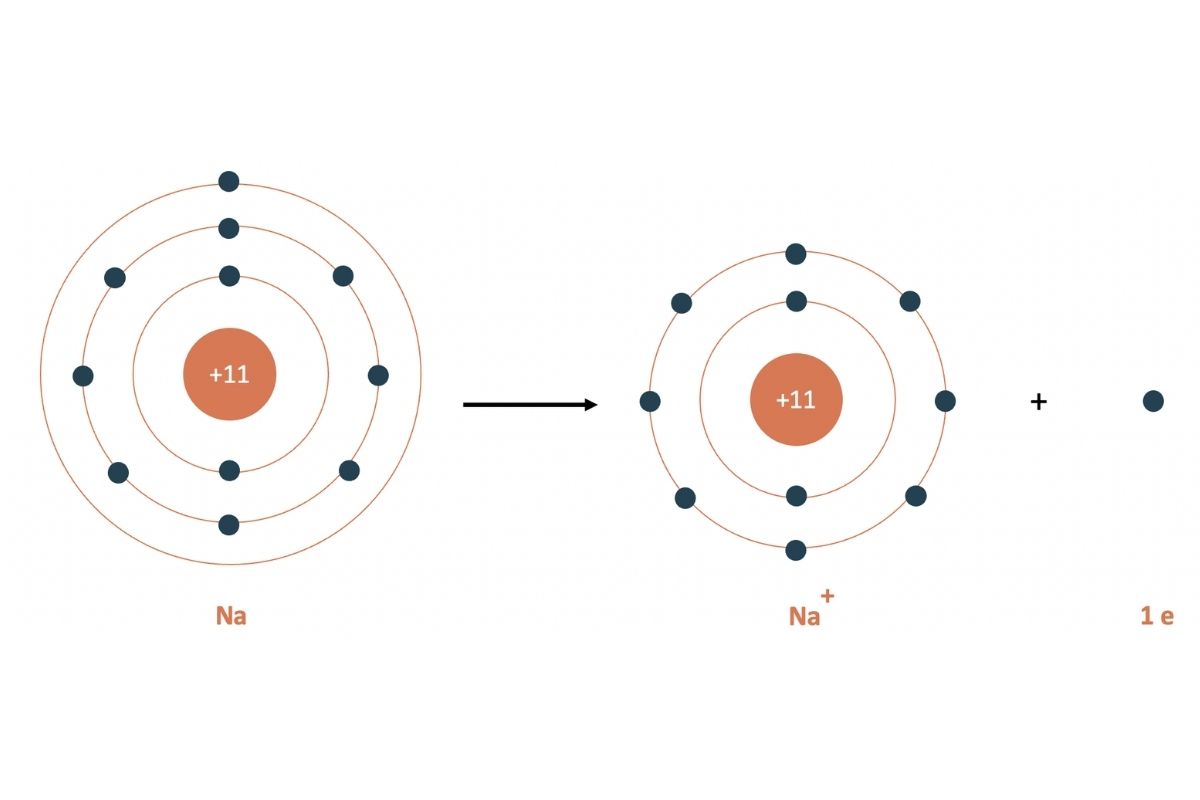
Dạng liên kết khi nguyên tử kim loại và phi kim tham gia trao đổi electron với nhau.
Chẳng hạn, trong NaCl, nguyên tử natri nhường một electron cho clo, tạo thành Na⁺ và Cl⁻. Hai ion này gắn kết với nhau thông qua lực hút tĩnh điện mạnh. Không chỉ giới hạn ở các ion đơn nguyên tử, liên kết kiểu này còn có thể xuất hiện trong các chất chứa ion đa nguyên tử như NH₄⁺ hoặc SO₄²⁻, tạo nên những chất như NH₄Cl hay MgSO₄. Chính nhờ kiểu liên kết đặc trưng này mà hợp chất ion có tính chất bền vững, dễ nhận biết qua khả năng dẫn điện khi tan trong nước hay điểm nóng chảy cao.
Đặc điểm vật lý và hóa học của hợp chất ion
Các chất được hình thành từ liên kết giữa các ion trái dấu thường có những đặc điểm vật lý và hóa học khá riêng biệt. Nhờ lực hút tĩnh điện mạnh giữa các ion trong mạng tinh thể, chúng thường tồn tại ở dạng rắn với nhiệt độ nóng chảy và sôi khá cao. Tuy nhiên, ở trạng thái rắn, các ion bị giữ chặt tại vị trí cố định nên không thể dẫn điện; chỉ khi nóng chảy hoặc hòa tan vào nước, các ion mới trở nên linh động và có thể truyền điện.
Mang cấu trúc mạng tinh thể làm cho các hợp chất này có điểm chung dễ tan trong nước, nhạt màu.
Cấu trúc mạng tinh thể giúp các chất này trở nên cứng, nhưng đồng thời cũng khiến chúng giòn và dễ vỡ khi chịu tác động cơ học. Hầu hết đều có màu sắc nhạt hoặc không màu, dễ tan trong nước và thường tham gia các phản ứng thông qua sự trao đổi ion, nhất là trong môi trường dung môi phân cực. Chính những đặc điểm này đã tạo nên tính chất của hợp chất ion, khiến chúng dễ nhận biết và có vai trò quan trọng trong nhiều quá trình hóa học.
Ứng dụng của hợp chất ion trong công nghiệp và đời sống
Các hợp chất mang ion giữ vai trò then chốt trong nhiều ngành công nghiệp và lĩnh vực đời sống, với mỗi lĩnh vực đều khai thác một khía cạnh riêng của loại chất này.
Trong ngành thực phẩm, Natri clorua (NaCl) không chỉ đơn thuần là gia vị mà còn là chất bảo quản truyền thống giúp ức chế sự phát triển của vi sinh vật. Tính tan tốt trong nước và khả năng tạo môi trường có áp suất thẩm thấu cao là yếu tố khiến NaCl trở thành lựa chọn lý tưởng trong bảo quản thực phẩm, đặc biệt là thịt, cá và rau củ muối.
Ngành xây dựng cũng tận dụng các chất mang ion như canxi cacbonat (CaCO₃), thành phần chính của đá vôi. Chất này được dùng để sản xuất xi măng, vữa và bê tông. Khi nung đá vôi, phản ứng phân hủy tạo ra CaO – nguyên liệu chính phản ứng với nước và silica trong quá trình đông cứng của xi măng, góp phần tạo nên độ bền cho các công trình.

Các hợp chất này có vai trò then chốt trong nhiều ngành công nghiệp và lĩnh vực đời sống.
Trong y học, các dung dịch điện giải như natri clorua sinh lý (NaCl 0,9%) hay magiê sunfat (MgSO₄) đóng vai trò thiết yếu trong điều trị mất nước, rối loạn điện giải và co giật. Sự hiện diện của các ion trong những dung dịch này giúp khôi phục cân bằng nội môi và đảm bảo hoạt động bình thường của hệ thần kinh, cơ và tim mạch.
Cuối cùng, trong ngành công nghiệp năng lượng, các hợp chất ion như muối nóng chảy (thường là hỗn hợp NaNO₃ và KNO₃) được sử dụng làm chất truyền nhiệt trong nhà máy nhiệt điện mặt trời. Ngoài ra, các dung dịch điện phân chứa ion cũng là thành phần cốt lõi trong hoạt động của pin, ắc quy và thiết bị lưu trữ năng lượng, nhờ khả năng dẫn điện hiệu quả khi ion tự do di chuyển trong dung môi.
Cách tổng hợp hợp chất ion trong phòng thí nghiệm
Trong môi trường phòng thí nghiệm, việc tạo ra các chất có bản chất ion thường được thực hiện thông qua phản ứng giữa kim loại và phi kim, hoặc giữa các dung dịch chứa ion dương và ion âm. Chẳng hạn, khi trộn dung dịch NaOH với HCl, ta thu được muối ăn NaCl cùng với nước – một ví dụ điển hình cho phương pháp tổng hợp đơn giản và hiệu quả.
Đối với những chất có cấu trúc phức tạp hơn, các nhà hóa học thường áp dụng các phản ứng trao đổi ion hoặc tạo kết tủa từ dung dịch chứa các ion tương ứng. Khi tạo thành các hợp chất ion trong những trường hợp này, việc kiểm soát chặt chẽ các yếu tố như nhiệt độ, nồng độ hay độ pH là điều kiện cần thiết để thu được sản phẩm tinh khiết và đạt hiệu suất cao.
Hợp chất ion có mặt ở đâu trong cuộc sống hàng ngày?
Trong đời sống hàng ngày, các chất có bản chất ion xuất hiện một cách quen thuộc và không thể thiếu. Từ muối ăn được sử dụng trong bữa cơm, các loại muối khoáng bổ sung dinh dưỡng, đến phân bón hỗ trợ cây trồng phát triển – tất cả đều là những ứng dụng thiết thực của loại chất này. Trong lĩnh vực y học, dung dịch NaCl sinh lý hay MgSO₄ thường được dùng để bù nước, cân bằng điện giải hoặc hỗ trợ điều trị một số bệnh lý.
Không chỉ dừng lại ở thực phẩm và y tế, các sản phẩm gia dụng như xà phòng, chất tẩy rửa hay các vật liệu xử lý nước thải cũng đều có sự góp mặt của các chất mang ion. Những ứng dụng như vậy chính là ví dụ về hợp chất ion có mặt khắp nơi trong cuộc sống, góp phần duy trì hoạt động sinh lý bình thường của cơ thể và đảm bảo vệ sinh, an toàn cho môi trường sống.
Nhờ vào cấu trúc và tính chất đặc trưng, các chất ion đã trở thành nền tảng quan trọng trong khoa học và công nghiệp. Việc nghiên cứu sâu hơn về chúng không chỉ mở ra cơ hội phát triển công nghệ mới mà còn nâng cao chất lượng cuộc sống. Sự hiện diện rộng rãi trong đời sống chứng minh tầm quan trọng không thể thiếu của những liên kết này.


